Новости
Аллергология: обзор отечественных публикаций. Сентябрь-2023

Фото из открытого источника (Яндекс-картинки)
-
 30.09.2023
30.09.2023
-
 779
779
Здравствуйте, уважаемые коллеги. Сегодня вашему вниманию предлагается обзор публикаций отечественных авторов за последние месяцы.
1. Оценка тяжести острых аллергических реакций (Рубан А.П.)
Введение. Актуальность разработки и внедрения в практику системы градации тяжести острых аллергических реакций (ОАР) обусловлена рядом составляющих. Во-первых, ростом числа ОАР и, соответственно, финансовых затрат на оказание помощи пациентам. Во-вторых, актуальность разработки методики обусловлена разнообразием клинических проявлений и степеней тяжести ОАР (в т.ч. анафилактических), требующих их унификации как для клиницистов, так и для исследователей. В-третьих, эти разработки помогут пациентам лучше понимать свое состояние здоровья, а также облегчат врачам коммуникации с ними (будет проще и доступнее объяснять лицу, перенесшему ОАР, его аллергостатус).
Цель: ознакомить с новыми подходами оценки степени тяжести ОАР, разработанными экспертами Американской академии аллергии, астмы и иммунологии (AAAAI) в 2021 г. Опробовать методику оценки тяжести ОАР на собственной выборке пациентов, оценить эффективность работы метода.
Методы: анализ клинических признаков ОАР 14 детей в возрасте от 11 месяцев до 16 лет с применением системы градаций тяжести, предложенной экспертами AAAAI 2021 г.
Результаты. Система оценки тяжести острых аллергических реакций представлена на рисунке.
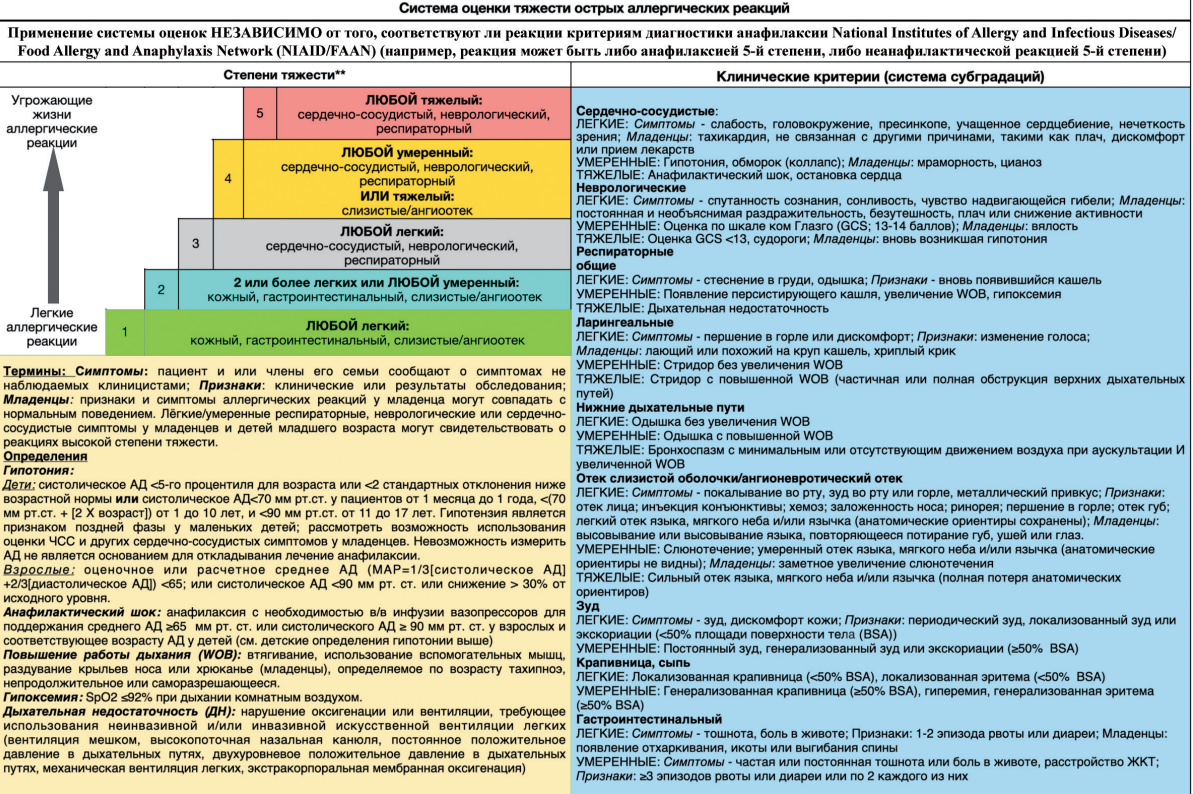
Оценка степени тяжести ОАР у пациентов предварительной выборки показала преобладание их градаций от 2 до 4 степени. При анализе клинических проявлений ОАР у данных пациентов симптомы с субградацией «тяжёлые» не выявлены по всем категориям систем органов. Симптомы поражения слизистых/наличие ангионевротического отёка присутствовали у всех пациентов, но в большинстве случаев не определяли степень тяжести реакции. Так называемые «жизнеугрожающие» категории симптомов (сердечно-сосудистые, неврологические, респираторные) как классификаторы применялись наиболее часто и позволяли более чётко классифицировать ОАР по степени тяжести.
Заключение. Таким образом, предложенная система оценки тяжести ОАР представляет собой новый удобный инструмент в руках практикующих специалистов (аллергологов-иммунологов, врачей-реаниматологов, врачей других специальностей) для корректного описания статуса пациента с последующим принятием решения о тактике его ведения (оказания неотложной помощи, объёма обследования, дальнейшего наблюдения), а также исследователей для унифицированного описания результатов наблюдения за пациентами или сообщения о неблагоприятных событиях при клинических испытаниях. При оценке тяжести ОАР в большом массиве данных анализ требует значительной затраты времени. Вероятно, для более удобного использования системы градации потребуется автоматизация процесса в виде создания калькулятора оценки тяжести ОАР в формате приложения для смартфона и/или персонального компьютера. Дальнейшее усовершенствование системы оценки тяжести ОАР путем включения в перечень категорий позиции «биомаркеры» позволит расширить её применение в клинической практике и научной сфере, усовершенствовать организацию медицинской помощи пациентам с ОАР.
Цель — оценить возможность применения крема с 5%-м филагринолом («Адмера») у детей (0–18 лет) в качестве эмолента при атопическом дерматите (АтД) и получить инструментальные данные об увлажненности кожи.
Материалы и методы. Открытое интервенционное исследование в параллельных группах детей с АтД 0–18 лет (n=72, медиана возраста 6 [3,75; 7,0] лет). 2 равные группы: 1-я получала крем метилпреднизолона 1 р/сут на очаги поражения в течение 14 дней + эмолент «Адмера» на остальную кожу; 2-я группа — аналогичное лечение + крем с 5%-м филагринолом наносился начиная с 5 дня на очаги поражения.
Результаты. Стандартная терапия применением топического глюкокортикостероида в комплексе с эмолентом была эффективна. Индексы тяжести на фоне лечения стероид + эмолент достоверно снижались: EASI 11,5 [6,0; 17,0] vs 2 [1; 3,8] балла, p<0,001; площадь поражения кожи с 17,5% [10,0; 26,8%] до 3,5% [1,25; 6,0%], p<0,001; оценка IGA 2 [2; 3] vs 1 [1; 2], p<0,01. Оценка общего зуда при АтД (max 10) на фоне терапии стала достоверно меньше: ночной зуд снизился c 3 [1; 7] до 1 [1; 3] и дневной зуд с 4 [3; 7] до 2,5 [1; 4] баллов, p<0,01.
Средние применения аппаратно измеренной увлажненности кожи вне очагов поражения исходно составили 8 [6,0; 12,0] ЕД. После 14 дней эмолента увлажненность сухой чистой кожи увеличилась до 10 [8,0; 15,0] ЕД (p=0,017). Увлажненность кожи на пораженных участках достоверно повысилась с 8 [6; 10] до 12,0 [8; 15] ЕД (p=0,001). Органолептическая оценка крема пациентами составила 4,48 балла (max 5).
В ходе настоящего исследования не было зарегистрировано случаев развития нежелательных явлений (НЯ), отвечающих критериям серьезной или умеренной силы реакции. 11,3% пациентов отмечали проявления кожного зуда, который быстро купировался без лечения.
Заключение. Крем с 5%-м филагринолом («Адмера») достоверно повышает увлажненность кожи, измеренную инструментально в области высыпаний и сухой кожи без очагов дерматита. Крем не вызывает значимых побочных реакций и может использоваться совместно с топическими стероидами.
Введение. Атопический дерматит (АД) является наиболее распространенным хроническим воспалительным заболеванием кожи у детей, которое значительно влияет на качество жизни ребенка и семьи в целом. Атопический дерматит рассматривается как заболевание, клинические проявления которого генетически детерминированы и обусловлены дефектом барьерных функций кожи и развитием иммунных реакций. Особенностью атопического дерматита является раннее начало, склонность к рецидивированию, формированию резистентных к терапии форм. Поэтому назначение лечения, позволяющего достичь контроля над симптомами заболевания, снизить риск тяжелого течения заболевания, является важным при ведении пациентов. Наружная терапия атопического дерматита предполагает назначение топических глюкокортикостероидов, роль которых трудно переоценить. Тем не менее длительная история применения препаратов данной группы показала возможность развития побочных реакций. В связи с этим правильный выбор препарата для лечения атопического дерматита у детей, обладающего высокой эффективностью и профилем безопасности, является основой для достижения ремиссии заболевания и преодоления кортикостероидофобии. Препаратом, соответствующим требованиям, предъявляемым к наружным топическим глюкокортикостероидам, обладающим высокой терапевтической эффективностью и безопасностью, является метилпреднизолона ацепонат, который рекомендован для лечения пациентов с атопическим дерматитом с 4-месячного возраста.
Основная часть. В работе представлены современные данные, подтверждающие оптимизированный профиль эффективности/безопасности метилпреднизолона ацепоната с минимальными местными или системными побочными эффектами. Как показывают исследования, новые отечественные препараты метилпреднизолона ацепоната (Комфодерм К) хорошо зарекомендовали себя в клинической практике.
Авторы провели анализ структуры госпитальной заболеваемости за период 2020–2022 гг. детей с аллергическими заболеваниями кожи, госпитализированных в аллергологическое отделение Детской республиканской клинической больницы Минздрава Республики Татарстан. Преобладающей нозологической формой в структуре аллергических заболеваний кожи являлся АД: в 2020 г. был госпитализирован 201 ребенок с АД (95,3%), в 2021 г. лечение по поводу АД получили 206 детей (91,5%), а в 2022-м – 186 пациентов (93,5%). Закономерно, что среди детей с АД, находящихся на стационарном лечении в аллергологическом отделении, преобладали пациенты со среднетяжелым и тяжелым течением АД. В исследовании 85 детей с АД (45,7%) в качестве базисной противовоспалительной терапии получали препарат метилпреднизолона ацепонат, 45 пациентам (24,2%) был назначен комбинированный препарат (бетаметазон, гентамицин, клотримазол), у 56 детей (30,1%) был использован препарат гидрокортизона бутират. Таким образом, приведенные данные свидетельствуют о том, что из всех ТГКС, используемых в программе лечения АД у детей различного возраста, независимо от степени тяжести заболевания, преобладающим является препарат метилпреднизолона ацепонат, что, очевидно, обусловлено высокой эффективностью и безопасностью препарата, доказанной в условиях реальной клинической практики. Эти характеристики препарата авторы проиллюстрировали тремя клиническими примерами.
Заключение. Топические кортикостероиды занимают значимое место в лечении атопического дерматита у детей. Метилпреднизолона ацепонат (Комфодерм К) обладает высоким профилем эффективности и безопасности при лечении АД у детей в возрасте старше 4 мес., в том числе при распространенных формах кожного процесса. Включение в состав препарата компонентов, восстанавливающих барьерные свойства эпидермиса, позволяет снизить риск повторного обострения и в целом повышает качество жизни пациентов.
Введение. Возможность развития хронической болезни почек (ХБП) при бронхиальной астме (БА) была показана ранее с помощью оценки скорости гломерулярной фильтрации. Было показано, что цистатин С можно рассматривать как показатель скорости гломерулярной фильтрации, однако результаты использования цистатина С в этом качестве при БА неоднозначны и требуют дальнейшего изучения и анализа.
Цель исследования – определить уровни цистатина С в сыворотке крови при различных клинико-патогенетических вариантах БА и сопоставить их с клинико-функциональными и лабораторными показателями, характеризующими БА и ХБП.
Материалы и методы исследования. Авторами было обследовано 52 больных бронхиальной астмой (с аллергическим вариантом бронхиальной астмы (АБА) – 30 больных, а в группу с неаллергическим вариантом заболевания (НАБА) входило 22 пациента). Расчёт скорости клубочковой фильтрации (рСКФ) производился по формуле CKD-EPI. Концентрацию цистатина С в сыворотке крови определяли методом иммунотурбидиметрии, использовали набор реагентов для определения специфических белков «Cystatin C FS» («Diasys», США).
Результаты. Выявлено, что уровень цистатина С в сыворотке крови находился в пределах нормальных величин при обоих вариантах БА, а средние значения рСКФ были существенно ниже при НАБА варианте по сравнению с АБА. При НАБА была выявлена значимая обратная корреляционная связь между уровнями цистатина С и рСКФ. Корреляционный анализ позволил выявить обратную связь уровней цистатина С с рядом показателей функции внеш[1]него дыхания, прежде всего, со скоростными показателями (МОС50выд, МОС75выд). Установлена разнонаправленная корреляционная связь уровня цистатина С с уровнем общего IgE: прямая – при АБА и обратная – при НАБА. Выявлена прямая корреляция между уровнем цистатина С и курсовой дозой парентерального глюкокортикоидного препарата.
Заключение. Полученные данные свидетельствуют о том, что оценка уровня цистатина С как индикатора СКФ при бронхиальной астме целесообразна, по-видимому, только при неаллергическом варианте заболевания.
Это была последняя статья обзора. До новых встреч.

